私たちの研究室での新しいワクチン開発への取り組み
ワクチンの研究

ワクチンは1000年以上前から病気の予防法として使われてきた伝統的な方法です。近代ではルイ・パスツールが様々な病気に対するワクチンを開発し、その手法は18世紀のエドワード・ジェンナーから続いている伝統的な方法だとして世に紹介されました。
治療薬と違いワクチンは健康な人に接種することと、ワクチンを受けた後には発熱などの症状がでることは少なくないため、その是非については古くから議論があります。また、インフルエンザなどでは高齢者の死亡率が高いため予防接種が大切ですが、高齢者ではワクチンの予防効果が十分でないという問題があります。一方で新型コロナウイルスワクチンでは変異株への対応が必要であったり、RNAワクチンという新しいワクチンも開発されたりしています。私たちの研究室ではこのようなワクチンに関する問題に取り組み研究を進めています。
新型コロナワクチンについての臨床研究
新型コロナワクチンは世界で使われ日本でも多くの人がワクチンを接種しています。使用されているワクチンはRNAワクチンと呼ばれるタイプのワクチンです。このRNAワクチンはこれまでのワクチンと比較すると副反応が強い傾向があります。そこで私たちはこの副反応についても臨床研究をしました。臨床研究は下の図に示す流れで実施しています。
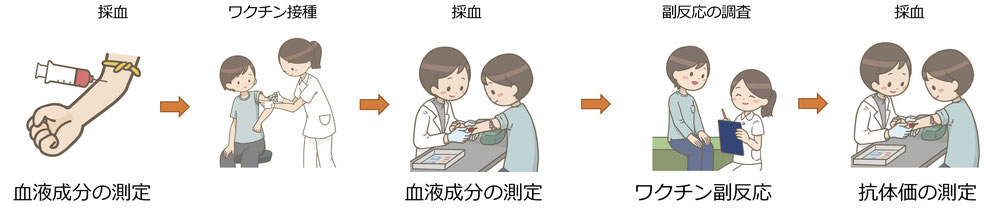
2020年の春の医療従事者向け新型コロナワクチン接種について、ワクチンの接種前と後に採血し血液の成分がどのように変化するのかを測定しました。また、その成分と副反応の強さとの関連を調べました。まず、1回目と2回目の副反応について調べると、下の図に示すように、2回目の方が、1回目よりワクチンの副反応が強いことがわかります。

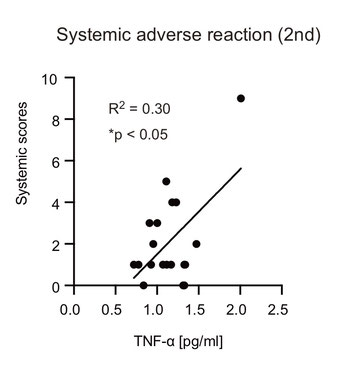
次にワクチンの副反応の強さと関連する血液の成分を調べてみました。すると、免疫の細胞から分泌される炎症性サイトカインと呼ばれるタンパク質の中で、TNF-αと呼ばれる炎症性サイトカインの血中濃度と副反応の強さが相関することがわかりました。
副反応とサイトカインの関係
左の図は2回目のワクチン接種1日後に測定した血中のTNF-αの血中濃度を横軸にとり、縦軸には発熱や頭痛などの全身性の副反応の強さを数値化したものです。
図に示されているとおりワクチン接種1日後に血液中のTNF-αと呼ばれる炎症性サイトカイン濃度が高くなると、全身性の副反応が強くなることがわかります。
縦軸のSystemic score: 発熱や頭痛などの全身性の副反応の強さを数値化した値。
横軸はワクチン接種後の血中のTNF-αの濃度
TNF-αはT細胞などから分泌されますので、TNF-αの血中濃度が高いことはT細胞の活性化が強いことがわかります。つまり、新型コロナワクチンを接種した後に副反応が強い人の体内では活発にT細胞が免疫応答をしていると推測されます。その他の成分として、「細胞外小胞内マイクロRNA」と呼ばれる分子の血中濃度と、副反応の強さが相関することもわかりました。
右の図では、miR-92a-2-5pという名前の「細胞外小胞内マイクロRNA」の血中濃度が低いと、ワクチン接種箇所が赤くなったり、あるいは接種後の頭痛や関節痛が強くでる可能性が高いことがわかります。
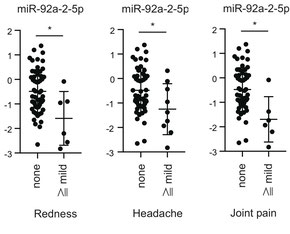
図の縦軸は「細胞外小胞内マイクロRNA」の濃度を示します。noneは副反応の症状が無かった人。mildは副反応の症状があった人。(Redness: 赤み、Headache:頭痛、Joint pain:関節痛)
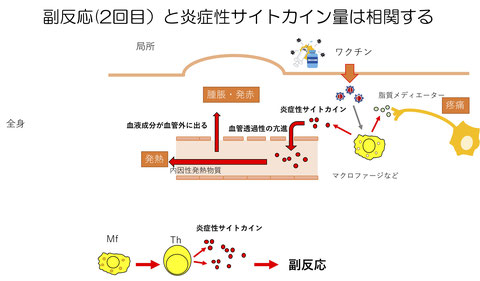
様々なワクチンの副反応の多くは免疫応答が原因であるといわれています。インフルエンザワクチンなどで生じる副反応の原因となる免疫応答のメカニズムの一部を右の図に示しています。
ワクチンを接種すると、接種した部位でTNF-αなどのサイトカインが分泌されることで血管の内皮細胞が活性化して、血液の液体成分が血管から組織へと漏れ出すことで腫れや赤みの原因となります。あるいは、このTNF-αの血中濃度が高くなると脳の視床下部で発熱のシグナルが入ります。また、このTNF-αは局所やリンパ節にいるT細胞からも分泌されます。今回の新型コロナワクチンの副反応の研究では、従来のインフルエンザワクチンなどと同じように、新型コロナワクチンの副反応も同じメカニズムで生じていることが予想されました。
まとめ
今回の研究では、従来から指摘されているとおり、新型コロナワクチンの副反応の強さは炎症性サイトカインとして知られるTNF-αが原因の一つであると推測されます。一方で、新しい発見として、副反応の強さと関連する成分として「細胞外小胞内マイクロRNA」を発見することができました。今後、この新しく発見した成分をもとに、副反応が軽減された新型コロナワクチンの開発につながると期待しています。詳しくは、プレスリリースと論文を参考にしてください。

(注)上の図は今回の研究の成果を一般の人向けに解説したものです。TNF-αはT細胞以外にもマクロファージなどの細胞からも分泌されます。T細胞はワクチンの成分に直接反応するわけではなく、抗原提示細胞が提示した抗原により活性化します。詳しくは論文またはプレスリリースをご覧ください。また、内容について問題があると思われた方はご連絡いただければ修正するようにいたします。
高齢者向けワクチンの開発

インフルエンザによる死亡の多くは65歳以上です。そのため高齢者にとってインフルエンザワクチンは非常に重要です。しかし、老化することで免疫力が低下しワクチンの予防効果も十分に現れないことが知られています。私たちの研究者ではその原因について調べました。老化したマウスを用いた動物実験から、ワクチン接種による炎症が強すぎることが原因となりワクチンによる予防効果が低下することがわかりました。そこで、この強すぎる炎症を抑えるためにmicroRNA192と呼ばれる小さなRNAをワクチンに添加することで老化したマウスの特異抗体価が回復しインフルエンザワクチンに対する予防効果が強くなることがわかりました(Tsukamoto H et al iScience 2020)。
このmicroRNA192を含むインフルエンザワクチンを作ることで高齢者にも高い予防効果のあるワクチンができると期待されます。また、インフルエンザワクチンだけでなく、成人用肺炎球菌ワクチンや新型コロナウイルスワクチンにも応用できるかどうかを現在調べています。
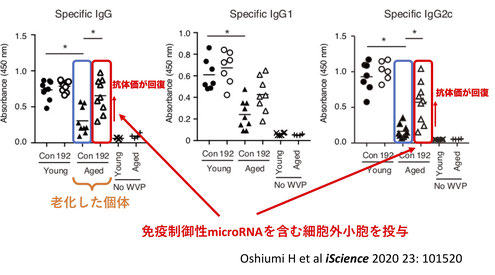
実験動物のC57BL/6のマウスでも、老化することでワクチン接種後の抗体価が若いマウスと比較して低迷しています。miR-192を含む細胞外小胞を老化したマウスに投与することで、ワクチン接種後の抗体価を若いマウス並みに回復させることができました。(特許出願済み)
HPVワクチン(子宮頸がんワクチン)と副反応
HPVワクチンは子宮頸がんを予防するワクチンとして日本でも承認されています。しかし、副反応への不安から多くの人がHPVワクチンの予防接種を受けるべきかどうかについて迷い、ワクチンの接種率が低下しています。
ワクチン接種後の重大な副反応としてどのようなワクチンでも、頻度が非常にまれではありますが、ギラン・バレー症候群や急性散在性脳脊髄炎などの副反応があります。そして、HPVワクチンを接種した後にこのような副反応があったのではないかと指摘する声もあります。このようなギラン・バレー症候群や急性散在性脳脊髄炎は最近の研究からは神経系に対する自己免疫応答として考えられるようになっています。また、これはワクチンに特有の現象ではなくウイルスが原因となる感染症でも極まれに生じることが知られています。
そこで、私たちはHPVワクチンが神経系に対する自己免疫応答を促進するのかどうかについて調べてみました。実験は、マウスの神経系に対する自己免疫疾患を誘導する実験的自己免疫性脳脊髄炎(EAE)と呼ばれる実験系を用い、わざとマウスに神経系に対する自己免疫疾患を誘導させ、自己免疫疾患の発症や重症化にHPVワクチンが悪影響を及ぼすかどうかを検討しました。

左の図はマウスにEAEを誘導し、同時にHPVワクチンのガーダシルとサーバリックスを投与した後の、神経系に対する自己免疫疾患の症状の程度を一ヶ月観察した結果になります。図のグラフの通り、HPVワクチンのガーダシルもサーバリックスもEAEでの神経系に対する自己免疫疾患には影響を及ぼさないことがわかりました(Nakashima M et al Scientific Reports 2021 11: 9369)

一方で、左の図のように血液の細胞外小胞内にあるmiR-451aの量が多いマウスは自己免疫疾患が重症化したのに対して、miR-451aが少ないマウスは自己免疫疾患の症状が軽症で済みました。この血液の細胞外小胞内のmiR-451aは健康なマウスやヒトでも緩やかに変動します。そのため、HPVワクチンの接種ではなく、miR-451aの量の違いが神経系に対する自己免疫疾患の発症に大きな影響を与えているのではないかと考えています。(Nakashima M et al Scientific Reports 2021 11: 9369)。

インフルエンザワクチンと副反応
ワクチンの副反応には局所での腫れや痛みだけでなく、非常に希有なケースとして、神経系に対する自己免疫疾患が生じることも指摘されています。
私たちの研究室では、この副反応が生じる原因や、何故、副反応が有る人と無い人がいるのかについて研究を進めてきました。実は私たちの身体のなかには、細胞外小胞(Extracellular vesicles)と呼ばれるウイルスほどの大きさの小さな小胞が血液の中を循環しています。この細胞外小胞内にあるmicroRNAとよばれる遺伝情報をもつRNAのバランスが壊れることと、副反応が生じることに関連があることがわかってきました。
例えば、miR-451aとmiR-16と呼ばれるmicroRNAのバランスの違いが、マクロファージが産生するサイトカインやケモカインの量に大きく影響を与えることを私たちは発見しました。

左の図の縦軸は、マクロファージが産生するサイトカインのIFN-βの量を示し、横軸は、血液の細胞外小胞内のmiR-451aとmiR-16のバランスを示します。このmiR-451a/miR-16の比と、サイトカイン量が逆相関することがわかります
(参照: Okamoto M et al JBC 2018 293: 18585-18600)
この他にも、miR-451aとmiR-16のバランスが変化することで、ワクチンの成分に対する免疫応答の強さが変化することが、動物実験などでわかってきました。詳しくは、上記の論文をご覧ください。
この細胞外小胞内のmiR-451aとmiR-16のバランスは数ヶ月かけてゆっくりと変動することもわかってきました。つまり、このバランスが大きく崩れることが、ワクチンの副反応の出方に影響をあたえているのではないかと考えて研究をつづけています。

左の図は、健康な人の血液中の細胞外小胞について、miR-451aとmiR-16のバランスの変化を経時的に調べたものです。
6人について120日間追跡調査をしたところ、最初の1週間では殆ど変換していません。しかし、一ヶ月たつと、2倍以上変化する人が一人現れ、3ヶ月後には、6人中の5人以上が、2倍以上変化しました。
詳細に調べると、10倍以上変動することもあり、また健康な人の中では30倍ほど、バランスが異なります。このようなバランスの変化が、ワクチンの成分に対する免疫応答の強さに影響をあたえるのではないかと考えています。
(参照: Okamoto M et al JBC 2018 293: 18585-18600)
私たちはこのような成果を論文として発表して、特許も出願しました。現在は臨床研究をおこない、どのような副反応をどれぐらい正確に予測できるのかについての研究を進めています。ワクチンによる感染症予防効果に加えて、副反応が生じるメカニズムを解明することが、ワクチンへの正しい理解へと繋がり、これが、接種率の向上に繋がると私たちは期待しています。


左の図は、2018・2019インフルエンザシーズンに、ワクチンを受けた人の臨床データです。ワクチン接種前に血液を採取し、細胞外小胞のmicroRNA(miR-451aなど)を測定すると、ワクチンを接種したあとに生じる、痛み、痒み、赤み、腫れなどが生じるかどうかを予測できることがわかりました。
引用:Miyashita Y et al PLOS ONE 2019, 14(7): e0219510
図説明:
(C)33人について予め採血し、血液中の細胞外小胞内のmicroRNA量を測定しました。インフルエンザワクチン接種後の腫れ、痛み、赤み、痒みについてアンケート形式で質問し、その症状が複数有った人(Multiple)と一つ又は無かった人(Single or None)に分けてプロットしたところ、複数の症状が有った人(炎症が強かった人)はmicroRNA量が低下していました。
(D)microRNA量でグラフを描き直すと、microRNA量が低いと、複数の症状を示す人(炎症が強かった人)が8割ほどの高い値を示しました。

熊本大学
大学院生命科学研究部
大学院医学教育部
医学部医学科
免疫学講座
〒860-8556
熊本市中央区本荘1−1−1
TEL : 096-373-5135(研究室)
FAX: 096-373-5138
Department of Immunology,
Graduate School of Medical Sciences,
Faculty of Life Sciences,
School of Medicine
Kumamoto University
1-1-1, Honjo, Chuo-ku, Kumamoto, 860-8556 Japan
Tel: +81-96-373-5135
Fax: +81-96-373-5138
